Качественные реакции
(Урок химии в 8 классе)
Олися ЗАКИРОВА,
учитель химии высшей квалификационной категории средней школы №7 г. Арска
Тип урока: урок применения знаний, умений и навыков.
Формы работы: фронтальная, групповая.
Технологии, применяемые на уроке: технология проблемного диалога, исследовательская технология.
Цель урока: продолжить формирование представлений о качественных реакциях в химии (научиться отличать одни вещества от других с помощью качественных реакций).
Задачи урока:
обучающие:
– содействовать применению понятий «качественная реакция», «реагент на определяемое вещество», «индикатор»; сформировать понятие «аналитический сигнал»;
– продолжить формирование навыков грамотного выполнения химического эксперимента; повторить правила техники безопасности при проведении лабораторных работ;
развивающие:
– развивать навыки вести сравнительный анализ, обобщать и делать выводы, формулировать определения понятий;
– развитие логико-смыслового мышления учащихся, памяти, химического языка, а также умения осуществлять самостоятельную деятельность на уроке;
воспитательные:
– воспитывать культуру умственного труда, положительную мотивацию к учению;
– способствовать воспитанию дисциплинированности;
– продолжить формирование убеждения учащихся в необходимости привлечения средств химии к пониманию и описанию процессов, происходящих в окружающем мире.
Планируемые результаты обучения:
предметные: проводить химические опыты и эксперименты и объяснять их результаты.
Метапредметные:
регулятивные УУД:
– выдвигать и формулировать цели деятельности;
– планировать свою деятельность в соответствии с ее целью;
– самостоятельно осуществлять действия по реализации плана достижения цели;
познавательные УУД:
– строить логические рассуждения;
– решать исследовательским путем поставленную проблему, поиск и выделение необходимой информации;
– построение логической цепи рассуждений, описывать самостоятельно проведенные эксперименты, представлять информацию расписыванием;
коммуникативные УУД: понимать и воспринимать речь учителя, участвовать в совместном обсуждении результатов эксперимента;
личностные: осознание единства и целостности окружающего мира, возможности его познаваемости и объяснимости на основе химических знаний, развитие самостоятельности в приобретении новых знаний и практических умений.
Основные виды деятельности учащихся: учиться выявлять качественные превращения изучаемых веществ в ходе эксперимента и лабораторных опытов.
Методы: беседа, объяснение, самостоятельная работа, демонстрационный эксперимент (проблемный, ученический), лабораторная работа, решение задач (качественной, практико-ориентированной), проверочная работа.
Оборудование: компьютер, проектор, электронная презентация, выполненная в программе Power Point, раздаточный материал, реактивы и лабораторная посуда.
Технологическая карта урока
| Деятельность учителя | Деятельность учащихся |
| I. Этап мотивации (самоопределения) к учебной деятельности
Цель: проверка готовности учащихся, их настрой на работу |
|
| Приветствие учащихся, психологический настрой, включение в деловой ритм. | Подготовка к работе |
| II.Этап актуализации и фиксирования индивидуального затруднения в проблемном действии
Цель: подготовка мышления учащихся, организация ими внутренней потребности к построению учебных действий, фиксирование индивидуального затруднения. |
|
| Создание проблемной ситуации
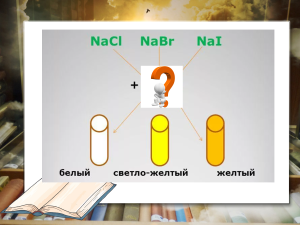
– Давайте посмотрим на экран. (На слайде –презентации.)
– Что мы можем найти общее в рисунке и какое различие? Какое вещество все объединяет? Отличать вещества друг от друга можно на основе каких-либо признаков или качеств. Есть вещества, которые несложно отличить друг от друга по внешнему виду, допустим цвету, или запаху. А есть вещества, которые невозможно отличить друг от друга по внешнему виду. Например, ювелирные изделия из платины и серебра. |
Учащиеся выдвигают гипотезы: Делают умозаключения, сравнения, выводы.
Отвечают на поставленные вопросы, опираясь на ранее полученные знания. |
| III.Этап постановки проблемы
Цель: организация анализа учащимися возникшей ситуации и выявление причины затруднения. |
|
| – Тогда проводятся специальные химические реакции, которые называются…
– Как называется это вещество? – Как называются такие реакции? – Попробуем сформулировать тему лабораторного практикума. Например, как бы вы отличили друг от друга серебряную и алюминиевую кружку?
– Какую цель мы должны решить сегодня на уроке? |
Формулируют и тему «Качественные реакции»
Ответы учащихся
– Весы сравнивать, выявить различия, определить признаки, качества… |
| IV. Этап фиксации знания знаний, умений и навыков
Цель: формирование умений у учащихся применения нового способа действий. |
|
| – Рассмотрим качественную реакцию. (На столе находятся колбы с газами: углекислым газом и кислородом.)
– Что мы можем сказать о наблюдаемых физических свойствах этих газов? – Давайте с помощью тлеющей лучинки определим, в какой колбе находится кислород, а в какой – углекислый газ. (Обнаружение кислорода и углекислого газа тлеющей лучинкой.) –В какой колбе кислород? – Может ли в углекислом газе вспыхнуть тлеющая лучинка? Какое применение углекислого газа основано на этом свойстве?
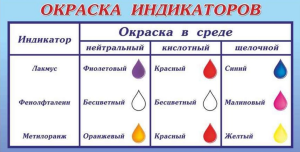
– Можем ли мы утверждать, что во второй колбе углекислый газ? Может быть здесь находится азот, ведь он тоже не поддерживает горения? Как доказать, что во второй колбе именно углекислый газ, а не азот? – В колбу с углекислым газом добавить небольшое количество известковой воды. – Выпадение осадка, выделение газа, которое может быть зафиксировано по появлению запаха, пузырьков газа в растворе при проведении качественных реакций называют аналитическим сигналом. Физкульминутка «Окраска индикаторов» (На партах лежат цветные карточки по цвету индикаторов в разной среде. Учитель называет вещества. Например, NaOH.)
|
Описание физических свойств газов.
– В колбе с кислородом тлеющая лучинка загорается. – В углекислом газе лучинка не может вспыхнуть, углекислый газ не поддерживает горение и поэтому используют для тушения пожаров.
Провести качественную реакцию.
Делают выводы.
Аналитический сигнал – явления при проведении качественных реакций, с помощью которых можно распознать вещества.
Ученики определяют цвет и встают дети, у которых синие, малиновые, желтые карточки и поднимают руки. |
| V. Выполнение практической части
Тема. Качественные реакции. Цель: провести качественные реакции и ознакомиться с их внешними проявлениями. (Проведен инструктаж по ТБ.) Оборудование и реактивы: таблицы «Растворимость кислот, оснований и солей в воде» и «Определение анионов и катионов», «Изменение окраски кислотно-основных индикаторов в зависимости от среды раствора (pН)», штатив с пробирками, пипетки, спиртовка, спички, набор реактивов для выполнения работ. Ход работы I вариант Задание 1. Две пробирки с бесцветными растворами сульфатов магния и калия Распознайте, в какой пробирке находится ионы магния. Задание 2. Две пробирки с бесцветными растворами бромидов меди и натрия. Распознайте, используя следующие растворы содержащие анионы: ОН—, F—, в какой пробирке, какое вещество. Задание 3. Две пробирки с бесцветными растворами хлоридов железа (III) и бария. Распознайте, используя следующие растворы содержащие анионы: Вr—, OH—, в какой пробирке, какое вещество. Задание 4. В склянке без этикетки находится бесцветный раствор. Предполагают, что это раствор фенолфталеина. Проведите опыт, подтверждающий или опровергающий это предположение. Задание 5. Дается анионы: NO32-, РO43- , OH— ; катионы : Ag+, К+ , NH4+ Провести возможную качественную реакцию между ионами. II вариант Задание 1. Две пробирки с бесцветными растворами хлоридов алюминия и бария Распознайте, в какой пробирке находится ионы бария. Задание 2. Две пробирки с бесцветными растворами нитратов серебра и натрия. Распознайте, используя следующие растворы содержащие анионы: Вr—, F—, в какой пробирке, какое вещество. Задание 3. Две пробирки с бесцветными растворами хлоридов хрома (III) и калия. Распознайте, используя следующие растворы содержащие анионы: Вr—, OH—, в какой пробирке, какое вещество. Задание 4. В склянках без этикеток находятся растворы: в одной – соляной кислоты, в другой – гидроксида лития. Как опытным путем определить, в какой склянке находится соляная кислота? Задание 5. Дается анионы: S2-, SO42- , SO32- ; катионы : Cu2+, Li+ , NH4+ Провести возможную качественную реакцию между ионами. На примере конкретных химических реакций рассмотрим качественные реакции. |
|
| VI. Этап закрепления
Цель: усвоение учащимися способа действия. |
|
| – На ваших столах лежат карточки с раскрасками
I вариант II вариант
– Раскрасьте рисунки в цвет получившегося осадка или цвета химической реакции по номерам заданий. (После выполнения проверяют по шаблону.) |
В рабочих листах каждый ученик фиксирует признаки и делает выводы.
|
| VII. Этап включения в систему системы знаний и повторения
Цель: повторение и закрепление изученного, выявление границы применимости нового знания и использование его в системе изученных ранее знаний. |
|
| Учитель анализирует работу класса, оценивает. Предлагает разноуровневые домашние задания по выбору, комментирует предложенные задания:
1-й уровень. Написать уравнения химических реакций, характеризирующих качественный состав хлорида меди (II). 2-й уровень. Cоставить тест по изученной теме или сделать подборку заданий по теме сегодняшнего практикума. 3-й уровень. Выполнить мини-проект «Качественные реакции в повседневной жизни» акцентируя внимание на явлениях, которые встречаются в трудовой деятельности ваших родителей, в домашнем хозяйстве. |
Подводят итог своей деятельности, высказывая, формулируют умения устанавливать значения результатов своей деятельности для удовлетворения своих потребностей, мотивов, жизненных интересов. |
| VIII. Этап рефлексии учебной деятельности
Цель: самооценка учащимися результатов своей деятельности. |
|
| – В конце нашего урока предлагаю вам составить синквейн на основе изученного материала.
1-я строка – назовите одно ключевое слово – существительное, определяющее содержание сегодняшнего урока. 2-я строка – придумайте прилагательное, раскрывающие это существительное. 3-я строка – назовите глаголы, определяющие качественные реакции 4-я строка – сформулируйте одно короткое предложение. 5-я строка – выразите свои чувства и ассоциации, связанные с понятием. – Сегодня мы говорили о том, насколько разные вещества. У каждого свой набор свойств, качеств. |
Слушают, задают вопросы на понимание и уточнение, участвуют в обсуждении, выражают собственное мнение о работе и полученном результате.
1. Реакция.
2. Качественные. 3. Изменяется, выделяется, меняется… 4.
5. |